Les cyanures, un poison cellulaire puissant et fortement réactif qui peut se rencontrer sous formes gazeuses, liquides et solides.
Les intoxications cyanhydriques sont dues à des substances susceptibles de libérer des ions cyanures (CN-). Les principales circonstances des intoxications ‘ par le cyanure sont les accidents du travail, les intoxications suicidaires et à l’inhalation de fumée d’incendie.
Selon leurs particularités chimiques et toxicologiques, les produits cyanogènes peuvent être classés en plusieurs groupes :
— groupe I: acide cyanhydrique, cyanogène et sels simples de l’acide cyanhydrique ;
— groupe II: dérivés halogénés de l’acide cyanhydrique ;
— groupe III : nitriles et substances organiques cyanogéniques ;
— groupe IV : dérivés cyanés dont la toxicité n’est pas liée à la libération d’ions CN-.
 Le système de thiosulfate sulfurtransufurase n’est pas nécessairement le mécanisme primaire de détoxification du CN décrit ci-dessus, parce que peu de thiosulfate pénètre la membrane mitochondriale pour accéder à l'enzyme de transférase.
Le rôle du soufre dans la détoxification est de convertir le CN en SCN, autres donneurs potentiels de soufre: polysulfures, thiosulfanates, polythionates, SCN inorganique, et soufre élémentaire associé aux protéines.
De façon générale il est possible que du soufre soit dérivé du mercaptopyruvate par l'intermédiaire de β-mercaptopyruate sulfurtransferase et les diverses formes de soufre de sulfane inter converti par rhodanese.
L’albumine plasmatique peut réagir par son soufre avec le cyanure et le complexe albumine plasmatique – cyanure sera un amortisseur primaire de détoxification.
Le système de thiosulfate sulfurtransufurase n’est pas nécessairement le mécanisme primaire de détoxification du CN décrit ci-dessus, parce que peu de thiosulfate pénètre la membrane mitochondriale pour accéder à l'enzyme de transférase.
Le rôle du soufre dans la détoxification est de convertir le CN en SCN, autres donneurs potentiels de soufre: polysulfures, thiosulfanates, polythionates, SCN inorganique, et soufre élémentaire associé aux protéines.
De façon générale il est possible que du soufre soit dérivé du mercaptopyruvate par l'intermédiaire de β-mercaptopyruate sulfurtransferase et les diverses formes de soufre de sulfane inter converti par rhodanese.
L’albumine plasmatique peut réagir par son soufre avec le cyanure et le complexe albumine plasmatique – cyanure sera un amortisseur primaire de détoxification.
 Elimination : Environ 80 % de la dose des cyanures sont excrétés sous forme de thiocyanates par voie urinaire lors d'intoxication à des doses faibles. L'élimination moyenne T1/2 pour SCN a été estimée à 2.7 jours chez les sujets en bonne santé et à 9 jours pour ceux avec l'insuffisance rénale.
Le cyanure est éliminé dans les urines, les fèces, la sueur et l’air expiré sous forme inchangée. Une partie des carbones de l’ion cyanure est éliminée par voie alvéolaire.
Elimination : Environ 80 % de la dose des cyanures sont excrétés sous forme de thiocyanates par voie urinaire lors d'intoxication à des doses faibles. L'élimination moyenne T1/2 pour SCN a été estimée à 2.7 jours chez les sujets en bonne santé et à 9 jours pour ceux avec l'insuffisance rénale.
Le cyanure est éliminé dans les urines, les fèces, la sueur et l’air expiré sous forme inchangée. Une partie des carbones de l’ion cyanure est éliminée par voie alvéolaire.
 Le cyanure se fixe à cet enzyme au niveau du fer ferrique Fe3+ de l’hème a3 et le cuivre A Cu2+
Il semblerait que l’ion cyanure ponte les ions fer et cuivre au sein du site actif. L’atome de carbone de l’ion cyanure est lié à l’atome de fer tandis que l’atome d’azote est lié à l’atome de cuivre. Le pontage serait donc binucléaire.
De même, il a été montré que la fixation primaire s’effectue sur le CuB 2+, et non sur le fer, bloquant ainsi le transfert d’électrons. La fixation du cyanure sur le cytochrome oxydase est réversible, ce qui permet d’expliquer le mode d’action et l’efficacité de certains antidotes.
Le cyanure se fixe à cet enzyme au niveau du fer ferrique Fe3+ de l’hème a3 et le cuivre A Cu2+
Il semblerait que l’ion cyanure ponte les ions fer et cuivre au sein du site actif. L’atome de carbone de l’ion cyanure est lié à l’atome de fer tandis que l’atome d’azote est lié à l’atome de cuivre. Le pontage serait donc binucléaire.
De même, il a été montré que la fixation primaire s’effectue sur le CuB 2+, et non sur le fer, bloquant ainsi le transfert d’électrons. La fixation du cyanure sur le cytochrome oxydase est réversible, ce qui permet d’expliquer le mode d’action et l’efficacité de certains antidotes.
 a- La solution de cyanure est chauffée (50 - 100 °C) avec le phosphate de pyridoxal en excès à pH neutre puis acidifié environ à pH 4.0. Ce traitement a eu comme conséquence un aspect d'une fluorescence forte.
Des spectres d'excitation et d'émission ont été enregistrés Leurs maximums ont existé à 320 et à 427 nanomètre, respectivement. La fluorescence était stable pendant plusieurs heures. (O. Suzuki 1982)
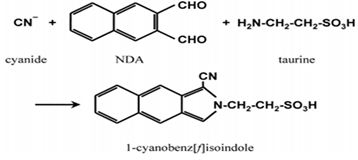
b- dérivatisation du cyanure avec le 2.3 naphthalenedialdehyde (NDA) et l'amine primaire taurine →dérivés fluorescent (Satoshi Chinaka 1998)
a- La solution de cyanure est chauffée (50 - 100 °C) avec le phosphate de pyridoxal en excès à pH neutre puis acidifié environ à pH 4.0. Ce traitement a eu comme conséquence un aspect d'une fluorescence forte.
Des spectres d'excitation et d'émission ont été enregistrés Leurs maximums ont existé à 320 et à 427 nanomètre, respectivement. La fluorescence était stable pendant plusieurs heures. (O. Suzuki 1982)
b- dérivatisation du cyanure avec le 2.3 naphthalenedialdehyde (NDA) et l'amine primaire taurine →dérivés fluorescent (Satoshi Chinaka 1998)
Toxicologie
Voies d’exposition
- Voie orale : L’ingestion d’hétérosides cyanogènes contenus dans diverse plantes Rosacée, Fabacée Poacée, Aracée
- Inhalation de fumées d’incendie : C’est actuellement la principale cause d’intoxication cyanhydrique.
- Suite à la projection de liquide (HCN, nitrile), surtout lorsque la peau est endommagée (plaies, brulure, ulcération…)
Toxicocinétique
- Absorption : très rapidement absorbés par inhalation (quelques secondes). 58% de l'acide cyanhydrique inhalé est retenu dans les poumons. L'absorption par voie orale est rapide (quelques minutes à quelques heures). La peau intacte ne permet que l’absorption d’HCN et des nitriles. Les sels hydrosolubles ne traversent que la peau lésée
- Distribution : rapidement distribué dans tout le corps. Dans le sang, l'ion cyanure est à une concentration deux fois plus élevée dans les globules rouges que dans le plasma. Bien que la liaison du cyanure à l’hémoglobine soit faible, elle existe et donne la cyanhémoglobine. Une concentration sanguine en cyanures d'environ 0,2 mg/100 mL est souvent associée à une intoxication sévère et au-delà de 0,3 mg/100 ml, elle est généralement mortelle. La demi-vie plasmatique des cyanures est estimée entre 20 minutes et 1 heure chez des sujets exposés à des doses non létales. Parmi les protéines plasmatiques, l’albumine est considérée comme le vecteur prépondérant de l’ion cyanure plasmatique.
Métabolisme
Le cyanure est rapidement détoxifié chez les mammifères ; par exemple, des taux de détoxification ont été estimés à 0.076 mg CN /kg/min chez les cobayes et à 0.017 mg CN/ kg /min chez l'homme. La voie principale de détoxification pour le cyanure est par transformation enzymatique en thiocyanate (SCN) moins toxique, qui est excrété par les reins. Il y a deux systèmes d'enzymes responsables du processus de transulfuration : *thiosulfate-cyanure transulfurase (rhodanese) *β mercaptopyruvate-cyanure - transulfurase . Rhodanèse : située dans des mitochondries et catalyse le transfert d'un atome de soufre à partir des donneurs de soufre aux accepteurs de soufre.![]()
Autres voies
Réaction avec la cystéine : Il Ya production de thiocyanoalanine , suivie de la fermeture de cycle et formation de l'acide 2 AminoThiazoline-4-Carboxylique (ATC) ou à son tautomère, acide 2 IminoThiazoline-4-Carboxylique qui est inerte. Combinaison avec l’hydroxocobalamine : La présence du métal Co dans cette métalloprotéine permet une liaison forte avec l’ion cyanure, quasiment irréversible dans les conditions physiologiques, en raison de la substitution d’un groupement hydroxyle par le radical cyanure bien plus nucléophile. Chaque molécule d’hydroxocobalamine est capable de fixer de manière équimolaire un ion cyanure en formant la cyanocobalamine, complexe stable d’élimination urinaire. Intégration de l’ion cyanure dans le métabolisme monocarboné L’intégration du carbone de l’ion cyanure dans le catabolisme des composés azotés monocarbonés est classiquement décrite, avec formation d’acide formique CN- + 2 H2O → HCOO- + NH3 Formation de cyanate Une faible partie du pool d’ions cyanures absorbés est oxydée en présence d’oxygène, en ions cyanates, sous forme de cyanates de sodium et de potassium. Les cyanates formés conduiraient in fine à la formation de dioxyde de carbone
Formation de cyanate
Mécanisme d’action toxique
La toxicité des agents cyanogènes est liée à leur capacité à libérer des ions cyanures (CN-) L’ion cyanure est un puissant poison cellulaire qui a la propriété de se lier à certains ions métalliques (fer, cuivre, cobalt…) inhibant au moins 40 enzymes différents, et plus particulièrement à l’ion ferrique de la cytochrome-oxydase mitochondriale servant au transport d'électrons dans la chaîne respiratoire pour former les molécules d'ATP l’organisme s’établit dans un ordre décroissant :hydroxocobalamine, méthémoglobine, cytochrome-oxydase et pigments respiratoires voisins, hémoglobine.- Rappel sur la chaine respiratoire mitochondriale :

Chaine respiratoire mitochondriale
Conséquences métaboliques de la toxicité du cyanure
L’inhibition de l’activité enzymatique de la cytochrome C oxydase est associée à un arrêt de la consommation d’oxygène par la cellule avec augmentation de la PO2 veineuse et à la déviation de son métabolisme vers la forme anaérobie, génératrice de peu d’énergie cellulaire (diminution du taux d’ATP et des rapports ATP/ADP et ATP/AMP) et d’acide lactique à l’origine d’une acidose métabolique précoce. La présence du lactate mène à une chute progressive du tampon endogène HCO3 plasmatique avec augmentation des ions H+. Le blocage énergétique produit par l’intoxication cyanhydrique altère précocement l’homéostasie calcique cellulaire, en augmentant le Ca intracellulaire. Cette augmentation de calcium intracellulaire a deux origines : une augmentation de l’influx calcique depuis le milieu extracellulaire et une mobilisation des réserves intracellulaires. L’augmentation du calcium intracellulaire dans un contexte d’ischémie, provoque un important relargage de neurotransmetteurs excitateurs comme l’aspartate et le glutamate. La libération accrue de ces acides aminés par l’ischémie est liée à un premier mécanisme classique d’exocytose calcium-induite. Le cyanure entraine une hyperglycémie due soit à :- une réponse aux catécholamines L’augmentation du calcium libre cytosolique observée au cours de l’intoxication cyanhydrique est associée à la libération massive de catécholamines (dopamine et noradrénaline) et aussi de glutamate
- stimulation de la gluconéogenèse par l’augmentation des lactates plasmatiques.
- augmentation d'activité de phosphorylase et donc la production de glucose dans le foie.
Clinique
La plus petite dose létale par ingestion est de 50 mg pour l’acide cyanhydrique et de 200 à 300 mg pour le cyanure de potassiumToxicité aiguë
La rapidité d’apparition de la symptomatologie est dépendante du produit en cause, de la voie d’absorption et de la dose ingérée.Toxicité chronique
En milieu professionnel, les signes de l’intoxication cyanhydrique chronique sont non spécifiques : céphalées, asthénie, troubles du sens olfactif et gustatif, vomissements et dyspnée à l’effort. De plus, des altérations de la fonction thyroïdienne (action inhibitrice des thiocyanates sur la captation de l’iode par la thyroide et son incorporation dans la molécule de tyrosine) et des taux bas de vitamine B12 et d’acide folique ont été observés au cours d’expositions professionnelles prolongéesTraitement
- prise en charge non spécifique, qui implique le maintien des fonctions vitales par l’utilisation des moyens de réanimation, et le traitement spécifique, soit l’utilisation des antidotes ou « anticyanures » spécifiques.
- Limiter l’exposition respiratoire
- Maintien des fonctions vitales
Analyse
Les tissus les plus appropriés pour l'analyse de cyanure sont le sang, le cerveau, le myocarde, le foie, les poumons, la rate, les reins, et le contenu gastrique. prélèvement avant l'administration de produits qui complexent les ions CN- La demi-vie courte du CN- sanguin (60-90 minutes). dosage rapidement après le prélèvement (dans les 24 heures) Réaction d’identification :- Réactions non spécifiques :
- La teinture fraîche de GAÏAC donne une coloration bleue par formation de tétragaïacoquinone.
- L’acétate de benzidine donne une coloration bleue.
- Le réactif de KASTLE-MEYER à la phtaline (incolore en milieu sodique) donnant une coloration rouge par réoxydation en phtaléine qui se manifeste grâce à l’alcalinité normale du réactif.



Dosage
- Méthodes colorimétriques :


- Méthodes chromatographiques :
Extraction
-Dans une fiole en verre hermétiquement fermée avec un couvercle. -0.2 ml de solution acide phosphorique 50 % est, injectée dans la fiole et puis chauffage à 50° C pendant 30 min pour l'extraction d'espace libre du cyanure. -Un volume de 0.5 ml de la vapeur d'espace est aspiré et injecté dans la colonne. Colonne : -colonne remplie : la capacité de résolution est fréquemment diminué par l'interférence des composants volatils contenus dans les spécimens biomédicaux ; -colonne capillaire de silice fondue est résistante à la dégradation et permet des mesures répétées sans vieillissement de la colonne. Détecteur : des niveaux toxiques du cyanure dans le sang peuvent être détectées par GC avec un FID, l'utilisation d'un NPD, d'un ECD et de la spectrométrie de masse donne des résultats satisfaisants. La limite de détection est environ 1 ng/ml permet des mesures de cyanure endogène dans le sang. Les concentrations toxiques et mortelles du cyanure dans le sang sont environ plusieurs µg/ml.- Fluorimétrie : (O. Suzuki 1982)
 a- La solution de cyanure est chauffée (50 - 100 °C) avec le phosphate de pyridoxal en excès à pH neutre puis acidifié environ à pH 4.0. Ce traitement a eu comme conséquence un aspect d'une fluorescence forte.
Des spectres d'excitation et d'émission ont été enregistrés Leurs maximums ont existé à 320 et à 427 nanomètre, respectivement. La fluorescence était stable pendant plusieurs heures. (O. Suzuki 1982)
b- dérivatisation du cyanure avec le 2.3 naphthalenedialdehyde (NDA) et l'amine primaire taurine →dérivés fluorescent (Satoshi Chinaka 1998)
a- La solution de cyanure est chauffée (50 - 100 °C) avec le phosphate de pyridoxal en excès à pH neutre puis acidifié environ à pH 4.0. Ce traitement a eu comme conséquence un aspect d'une fluorescence forte.
Des spectres d'excitation et d'émission ont été enregistrés Leurs maximums ont existé à 320 et à 427 nanomètre, respectivement. La fluorescence était stable pendant plusieurs heures. (O. Suzuki 1982)
b- dérivatisation du cyanure avec le 2.3 naphthalenedialdehyde (NDA) et l'amine primaire taurine →dérivés fluorescent (Satoshi Chinaka 1998)
- SAA indirect:
- Dans l’environnement :
- L’eau :
- Dosage :
- L’air :
- Prélèvement
- a) Pour HCN, le prélèvement est réalisé sur des tubes échantillonneurs contenant 2 plages d’adsorbant constitué de chaux en milieu basique. Ce type de prélèvement peut être conservé au moins 2 semaines à 25°C.
- b) Pour les sels de cyanure (NaCN et KCN essentiellement), le prélèvement est réalisé sur des filtres en PVC associés à des barboteurs de KOH 0,1 N. Ces échantillons sont à analyser dans les 5 jours au maximum.
- Intérêt : surveillance de l’exposition en milieu professionnel
- Le sol :
Was this article helpful?
YesNo
Last modified: 19 septembre, 2017




