Le monoxyde de carbone (CO) est le gaz toxique le plus fréquemment rencontré lors d’empoisonnements par les gaz. La formule chimique s'écrit CO. Ce corps composé est à l'état gazeux dans les conditions normales de pression et de température.
Il a comme caractéristique particulièrement sournoise de n’être pas décelable par nos sens ; il est incolore, inodore et très toxique pour les mammifères. c’est un poison invisible !
Le CO est issu de toutes les combustions et notamment des installations de chauffage non électrique et des moteurs à combustion. C’est pour cela qu’il est la cause de centaines d’accidents chaque année et plus particulièrement pendant l’hiver. Le CO est aussi la cause majeure de la toxicité des fumées d’incendies. Les activités professionnelles (gaz industriel ) peuvent mettre en présence des personnes avec le CO,c’est pour cela que des normes concernant le monoxyde de carbone et les activités professionnelles ont été établies. Il existe aussi une autre source anthropogénique non négligeable , responsable d’intoxication chronique c’et le TABAGISME avec ces différentes formes.
B- Détection et dosage du CO dans l'air alvéolaire expiré:
En ce qui concerne le dosage du CO dans l'air alvéolaire expiré, la formule de Ringold HbCO % = 0,5 + CO / 5) permet la conversion du résultat (ppm de CO dans l'air expiré) en % d'HbCO.
Méthode spectrométrique dans l'infrarouge
Le monoxyde de carbone a la propriété d'absorber le rayonnement infrarouge dans une zone proche de 4600 cm-1 ; il existe des appareillages automatiques (Onera type 80)
Methode électrochimique
Cette technique est basée sur l'utilisation de capteurs à pile dont la tension varie en fonction de la teneur en CO ; cette méthode a une sensibilité moindre que celle des techniques basées sur l'absorption de l'infrarouge.
Le taux de CO expiré est un bon reflet de l'intoxication tabagique récente (en dehors d'autres causes d'intoxication par le CO : d’où l’utilisation de l'analyseur de CO en consultation de sevrage tabagique.
aTWA = Threshold Weight Average
bTLV = Threshold Limit Value
cVEMP = Valeur d'exposition moyenne pondérée
dVECD = Valeur d'exposition de courte durée
VME – Valeur moyenne d’exposition
La valeur VME indique la concentration moyenne dans l’air des postes de travail en un polluant donné qui ne met pas en danger la santé de la très grande majorité des
travailleurs sains qui y sont exposés, et ceci pour une duré de 42 heures hebdomadaires, à raison de 8 heures par jours, pendant de longues périodes. Cette valeur correspond souvent au premier niveau d’alarme des appareils de détection. La VME ne représente pas une limite entre une concentration inoffensive et une concentration dangereuse.
VLE - Valeur limite d’exposition
-La valeur VLE complète la norme VME. En effet, la VME définit une valeur moyenne sur 8 heures et les concentrations de polluant varient souvent de façon considérable au cours du temps. Pour certains polluants, les dépassement de la valeur moyenne doivent être limité afin d’éviter une atteinte à la santé. Il est précisé que la valeur peut être atteinte 4 fois par jours pendant une durée de 30 minutes.
-Cette valeur correspond souvent au deuxième niveau d’alarme des appareils de détection.
-D'après les données issues du guide pour la qualité de l'air de l'OMS, la production endogène de monoxyde de carbone induit des taux variables entre 0,4 à 0,7% chez les sujets en bonne santé. Pendant la grossesse, ces taux s'élèvent à 0,7%-2,5%.
-Les niveaux de HbCO chez les personnes non-fumeuses oscillent habituellement entre 0,5 à 1,5% en fonction de la production endogène de monoxyde de carbone et des expositions environnementales. Des populations non-fumeuses qui sont soumises à certaines activités (automobilistes, policiers, travailleurs dans les tunnels, mécaniciens-auto, pompiers) peuvent supporter en chronique des taux dépassant 5%. Les gros fumeurs de cigarette peuvent dépasser 10% (OMS 1999).
-Afin de protéger les populations non jeunes atteintes de maladies coronariennes ainsi que les fœtus portés par des mères non-fumeuses contre les effets délétères par hypoxie, le taux de HbCO ne devrait pas dépasser 2,5%.
-Les valeurs guide de CO dans l'air et les périodes moyennes d'exposition ont été déterminées de manières à ce que le taux de HbCO n'excède pas 2,5%, et ce même lorsque des sujets normaux sous soumis à des exercices physiques légers ou modérés soit ( 1 mg/m3 = 0,86 ppm à 20°C) :
- 100 mg/m3 (86 ppm) pendant 15 mn*
- 60 mg/m3 (50 ppm) pendant 30 mn
- 30 mg/m3 (25 ppm) pendant 1 h
- 10 mg/m3 (8,6 ppm) pendant 8 h
Recommandations en milieu résidentiel et lieux publics
Propriétés physicochimiques
Dans les conditions ordinaires de pression et de température le CO est un gaz inodore, incolore et sans saveur, donc il est impossible de détecter le monoxyde de carbone (CO) par nos sens : c'est un fantôme qui tue !Propriétés physiques
- Un peu plus léger que l’air Avec sa densité de 0,968 (diffusion rapide dans l’atmosphère)
- Non irritant des voies respiratoires.
- Difficilement liquéfiable Le monoxyde de carbone à l'état liquide, est un liquide cryogénique à -191,5°C, il faut donc tenir compte de tous les aspects que comporte l'exposition à un liquide à très basse température.
- Il est peu soluble dans l’eau (2.3 ml dans 100ml d’H2O à 20°C)-àlipophile donc très absorbé par voie pulmonaire. Assez soluble dans certains solvants organiques tel que l’acétate d’ éthyle, éthanol, l’acide acétique.
- Non adsorbé par le charbon actif, donc les masques de charbon actif sont inefficaces.
- Absorbe dans l’IR d^'ointérêt dans la détection et le dosage.
- Masse molaire : 28.01 g/mol, * Pf : -207°C *Pe: -191°C * Densité du liquide (D4-195 ): 0.814.
- Densité du gaz (air 1) : 0.968 * T°d’auto inflammabilité : 609 à 700°C * A 25°C et 101KPa : 1 ppm = 1.14mg/m3.
Propriétés chimiques
- Il se dissocie en C et CO2 entre 400-700°C. A partir de 800°C l’équilibre 2CO ⇔ CO2 + C va dans la formation de CO. Si la T°< 400°C et dans la T0 ordinaire cette décomposition a lieu en présence de certains catalyseurs : Cr, Pd.
- Le CO brûle dans l’aire ou l’oxygène avec flamme bleue pour donner le CO2 avec dégagement de la chaleur.
- En raison de ses propriétés fortement réductrices, il peut agir avec les agents oxydants en formant des composés très explosifs.
- Il n’attaque pas les métaux à pression < 3500KPa, à plus haute pression il agit avec le Ni, cobalt, Cr en donnant des carbonyles très instables et toxiques
- En présence de nickel réduit et à 250 °C, le monoxyde de carbone peut être transformé en méthane :
![]()
Sources d’émission et Modes de formation
Les principales sources d’émission de CO sont liées aux activités humaines, dès lors qu’il existe une combustion incomplète de matières organiques. Il existe normalement dans l'air une très faible quantité de CO provenant de phénomènes naturels (0,01 à 0,2 ppm). La pollution par le CO provient essentiellement de combustions incomplètes, effectuées en présence d'une quantité insuffisante d'air (d'oxygène) (flamme instable ou touchant un corps froid), le carbone ne réagit donc pas complètement avec l’oxygène. Au cours d'une combustion, l'oxydation du carbone par l'oxygène se fait en deux étapes :C + O2 ↔ 2CO
2CO + O2 ↔ 2CO2
La première réaction étant beaucoup plus rapide que la deuxième, le CO est toujours formé, et ne disparaît que s'il y a assez d'oxygène pour que la deuxième réaction soit complète.Les modes de formation
Sources anthropiques * Sources liées au milieu intérieur (hors milieu professionnel à pollution spécifique) En milieu intérieur, le CO provient essentiellement de la fumée de tabac ou de l’utilisation d’un appareil non raccordé à un conduit de fumée, par exemple : cuisinières, chauffe-eau, barbecues, braseros, groupes électrogènes, chauffages mobiles d’appoint. Une production importante de CO peut être également générée dans les logements et leurs annexes par les appareils de chauffage et de production d’eau chaude défectueux, vétustes, raccordés à un conduit de fumée non-conforme ou non entretenu (tuyau de raccordement débouchant directement à l’extérieur, conduit de fumée fissuré, obstrué par les suies, …). L’utilisation d’un appareil dans de mauvaises conditions, tel qu’un chauffage d’appoint utilisé en continu, un moteur thermique utilisé dans des locaux insuffisamment ventilés, peut aussi D’une manière générale une ventilation insuffisante constitue une circonstance aggravante. Il est à noter que chaque année les incendies sont également responsables d’un nombre important de décès par intoxication au CO. * Sources domestiques : Les appareils domestiques à gaz (chauffe-eau, radiateurs) ou à charbon (poêles, braseros), produisent du CO et nécessitent donc la présence d'un système de renouvellement d'air efficace (en particulier amenées d'air permanentes obligatoires déterminées en fonction des caractéristiques des appareils à gaz). Ils peuvent être à l'origine de fortes teneurs en CO si l'aération du local est insuffisante et la combustion incomplète, par exemple si l'atmosphère est saturée en vapeur d'eau. L'absence d'odeur fait que rien n'alerte les personnes éventuellement exposées. Actuellement ni le gaz de ville ni le gaz domestique en bouteille (propane, butane) ne contiennent de CO, c'est bien lors de leur combustion incomplète que celui-ci se forme. Tabac : La fumée de tabac contient de l'ordre de 4 % (40 000 ppm) de CO et représente donc une source reconnue d'intoxication chronique au CO pour les fumeurs (oxycarbonémie de l'ordre de 8 à 9 % pour un fumeur de 20 cigarettes par jour), ainsi que d'exposition occasionnelle pour les personnes séjournant dans la même pièce qu'un fumeur, en milieu confiné (de l'ordre de 20 ppm dans une pièce enfumée). Sources liées au milieu extérieur En France, à l’heure actuelle, les transports routiers (moteurs à combustion interne) sont responsables d’un tiers des émissions totales de CO dans l’air extérieur, deux tiers des émissions de CO étant dus aux foyers fixes de chauffage et aux processus industriels (installation de chauffage et de production d’eau chaude, métallurgie, production de charbon de bois, production de papier, process chimiques, etc.). Cependant, les foyers fixes de chauffage et les dispositifs industriels interviennent moins que les transports routiers dans la pollution oxycarbonée des voies urbaines (lieux d’exposition humaine), car le CO est généralement émis en hauteur, au dessus des toitures, et est rapidement dispersé dans l’atmosphère. Sources mobiles : Il s'agit des moteurs de véhicules ou autres engins à moteur (compresseurs, etc.). Dans l'air extérieur, le CO que l'on mesure au niveau des voies respiratoires est pratiquement entièrement d'origine automobile (essentiellement véhicules à essence). Les teneurs varient en fonction de la distance aux sources (véhicules), des conditions du trafic et des facteurs de dispersion. Les teneurs maximales journalières correspondent aux pics de circulation du matin et du soir. Dans les grandes villes européennes, les teneurs moyennes sur 8 heures sont inférieures le plus souvent à 17 ppm et les maxima horaires peuvent atteindre 50 ppm. En France, les teneurs maximales horaires approchent 40 ppm sur les stations fixes implantées en bordure de certaines voies urbaines très fréquentées. Les teneurs mesurées par les réseaux de surveillance sont en baisse en raison de l'amélioration des émissions unitaires des véhicules pour ce polluant (en particulier extension du pot catalytique). Dans les ouvrages souterrains la teneur reste généralement inférieure à 100 ppm, si la ventilation est asservie au CO. Le suicide ou l'intoxication accidentelle par gaz d'échappement dans un local confiné (garage) entraîne la mort par intoxication à l'oxyde de carbone. Sources professionelles Elles sont variées, représentées par les véhicules, les combustions, les compresseurs et autres engins à moteur. L'exposition professionnelle au CO est elle aussi due à des combustions incomplètes, que ce soit le fait de moteurs (véhicules dans les garages, appareils d'entretien de la glace dans les patinoires), de fours ou chaudières à usages divers. Les fermentations de produits agricoles produisent également du CO. Le monoxyde de carbone peut se dégager lors de nombreuses activités industrielles.- métallurgie du fer et de divers autres métaux, leur raffinage par leurs composés carbonylés (ex. : nickel carbonyle), travaux de coupage et d'oxycoupage;
- synthèses chimiques : fabrication de carbure de calcium et des métaux carbonyles;
- emploi d'explosifs dans les mines et sur les chantiers hydroélectriques;
- travaux d'incinération des ordures dans les incinérateurs et les cimenteries;
- en métallurgie comme agent réducteur;
- dans l'industrie chimique pour la synthèse de nombreux composés : méthanol, acide acétique, acide formique, acide acrylique, phosgène;
- comme combustible.


Toxicocinétique
Absorption
La voie d’exposition principale est l’inhalation. Le monoxyde de carbone est facilement absorbé par les poumons. Du fait de sa très faible hydrosolubilité, le CO parvient rapidement au niveau des alvéoles pulmonaires ou il diffuse à travers la membrane alvéolocapillaire de façon similaire à l'oxygène. En présence d’une concentration constante pendant plusieurs heures, le taux d’absorption diminue régulièrement jusqu’à atteindre un état d’équilibre biologique entre la pression partielle de CO dans le sang des capillaires pulmonaires et de l'air alvéolaire.Distribution
- La plus grande partie du monoxyde de carbone absorbé se fixe de façon réversible aux pigments hèmes de l'organisme :
- Au moins 80 % se lie à l'hémoglobine des érythrocytes pour former la carboxyhémoglobine. L'affinité de l'hémoglobine pour le monoxyde de carbone est d'environ 240 à 250 fois supérieure à celle pour l'oxygène. Le CO inhibe ainsi la liaison de l’oxygène à l’hémoglobine ce qui diminue la libération d’oxygène dans les tissus (effet antagoniste de l’O2). Les organes et tissus à forte consommation en oxygène sont les plus sensibles à cette hypoxie : cœur, cerveau, muscles squelettiques, ainsi que le fœtus
- De 10 à 15 % réagit avec la myoglobine des cellules musculaires. La myoglobine a une constante d'affinité pour le monoxyde de carbone environ huit fois plus faible que celle de l'hémoglobine. La fixation du CO sur la myoglobine (protéine responsable du stockage de l’oxygène au niveau musculaire) affecte l’oxygénation de certaines cellules musculaires notamment au niveau du myocarde. Les cellules musculaires myocardiques retiennent plus le monoxyde de carbone que les cellules musculaires squelettiques (ratio 3:1).
- Une faible proportion (environ 5 %) peut aussi réagir avec les autres composés contenant de l'hème :métalloenzymes ; cytochrome-oxydases (dont l’a3 à l’origine d’une inhibition de la respiration mitochondriale), cytochromes P450 (CYP450), hydroperoxydases.La fixation du CO à ces protéines ne constitue pas pour autant un compartiment réservoir, aussi ce gaz n’a pas un effet toxique cumulatif.
- Le monoxyde de carbone traverse la barrière placentaire et la barrière hémato-méningée.
Métabolisme
- Le monoxyde de carbone n'est pratiquement pas métabolisé, moins de 1 % de la dose absorbée est oxydé en dioxyde de carbone.
- Il est aussi produit de façon endogène par l'organisme lors du catabolisme des pigments hèmes (de 0,5 à 1,0 ml de CO par heure chez l'adulte). Le niveau de carboxyhémoglobine endogène chez l'humain est évalué de 0,1 à 1,2 %. Les valeurs de référence de HbCO retrouvées dans la population générale sont :
- Le monoxyde de carbone est un métabolite du chlorure de méthylène et d'autres hydrocarbures halogénés.
Elimination
L’élimination du CO dépend des échanges respiratoires. Ainsi, La vitesse de diminution de l’HbCO dépend essentiellement de son taux initial après exposition et de la quantité d’oxygène disponible mais également de la variabilité individuelle, ce qui explique, les différences de résistance à une intoxication au CO observées au sein d’une population.- Le monoxyde de carbone est éliminé presque entièrement par ventilation pulmonaire dans l'air expiré.
- L'élimination se fait rapidement au début, puis devient plus lente avec le temps et lorsque la concentration de carboxyhémoglobine s'abaisse.
- La demi-vie de la carboxyhémoglobine chez l'humain est d'environ 3 à 5 heures pour un sujet en état de veille et au repos. Dans le cas d’un sujet endormi, elle peut dépasser 6 à 8 heures.
- Elle peut augmenter avec l'âge et diminuer avec l'activité physique.
- La demi-vie de la carboxyhémoglobine chez la femme enceinte est d'environ 3 à 4 heures tandis que celle du fœtus est d'environ 7 heures expliquant la gravité d’une intoxication chez une femme enceinte sans prise en charge rapide.
- Formation de carboxyhémoglobine (HbCO)
- Diminution du transport O2
- baisse de l’oxygène sanguin=hypoxémie et Hypoxie

Mécanismes d’action toxique
Le CO est principalement un poison sanguin :- Le principal mécanisme de l'action toxique est la liaison du monoxyde de carbone avec l'hémoglobine produisant la carboxyhémoglobine, ce qui a pour effet de diminuer la capacité de transport de l’oxygène du sang et d'interférer avec la libération tissulaire de l'oxygène. il y a compétition avec l’oxygène entraînant une hypoxie relative.
- Réduction de la libération d’oxygène au niveau cellulaire : déplacement de la courbe de dissociation de l’oxyhémoglobine (HbO2) vers la gauche suite à la modification allostérique de l’hème consécutive à la fixation du CO.
- Perturbation des mécanismes de respiration cellulaire par la fixation du CO aux cytochromes mitochondriaux.
- Dysfonction des cellules musculaires cardiaques et squelettiques à la suite de la fixation du CO sur la myoglobine.

- Hb + O2 ↔ HbO2
- HbO2 + O2 ↔ Hb(O2)2
- Hb(O2)2 + O2 ↔ Hb(O2)3
- Hb(O2)3 + O2 ↔ Hb(O2)4
- existe sous deux formes



Mécanismes de régulation du transport de l’O2
1) Effet Haldane : L’Hb a une affinité plus faible pour l’O2 quand les concentrations en CO2 augmentent. 2) Effet Bohr : L’affinité de l’Hb pour l’O2 diminue proportionnellement à la baisse du pH.
- Le diphosphoglycérate ↘l'affinité de l‘Hb pour l'oxygène.
- ↗de sa production chez les individus fréquentant les hautes altitudes, là où la PO2 est plus faible,pour faciliter la libération d'oxygène par les globules rouges.


- Liaison CO à Hb augmente affinité de Hb pour O2 restant ,déplacement courbe dissociation vers gauche
- Diminution pO2 très forte (85 mm Hg – de 100 à 15) nécessaire pour libérer 5ml O2 / 1OO ml sang
- Diminution relargage O2 au niveau tissulaire.
- aggravation hypoxie initiale

Symptômes de l’intoxication
Intoxications aiguës
- Le monoxyde de carbone est un asphyxiant chimique qui interfère avec la distribution de l'oxygène aux tissus et aux organes. Les organes ayant un besoin élevé en oxygène tels que ceux du système nerveux central et du système cardiovasculaire seront donc les premiers affectés. - Il n'existe pas de syndrome univoque évoquant à coup sûr une intoxication au CO. Même lorsque plusieurs personnes sont intoxiquées au cours du même incident, les signes peuvent être très divers. Le simple fait que plusieurs personnes ayant séjourné dans le même local se présentent avec des symptômes divers peut mettre sur la voie du diagnostic, ou au contraire entraîner des erreurs (analogie possible avec une intoxication alimentaire). - Le CO a été décrit comme « le grand imitateur » car les intoxications donnent lieu à un grand nombre de faux diagnostics de grippe, de gastro-entérites ou d’autres affections bénignes. Par ailleurs, les intoxications au CO se manifestent souvent en décompensant un mauvais état cardiaque ou cérébral sous-jacent. 2 phases- Phase d’imprégnation :
- Phase d’état :
- Au niveau neurologique
- Au niveau cardiovasculaire
- Autres troubles :
- Signes respiratoires : Polypnée sans cyanose, OAP lésionnel.
- signes musculaires de rhabdomyolyse
- teinte rouge '' cochenille '' de la peau, phlyctènes
- Effet reprotoxique
Intoxication chronique
-L'apparition d'effets toxiques résultant d'une exposition prolongée à de faibles concentrations de monoxyde de carbone n'est pas encore clairement établie dans la documentation scientifique. Le système nerveux central et le système cardiovasculaire seraient, tout comme pour les effets aigus, les cibles. -Divers symptômes tels que des maux de tête, de l'anorexie, de l'insomnie, des pertes de poids, de la faiblesse généralisée, des troubles de la mémoire et du langage ainsi que des déficits moteurs ont été rapportés. -Les études épidémiologiques réalisées chez divers types de travailleurs (inspecteurs de véhicules moteurs, surveillants de ponts et tunnels, mécaniciens automobiles, travailleurs de fonderie) n'ont pas réussi à démontrer qu'une exposition au monoxyde de carbone puisse provoquer une augmentation de la mortalité due aux maladies cardiovasculaires. -Pas plus que pour les fortes teneurs, l'intoxication à de faibles teneurs de CO ne présente d'aspect cliniquement caractéristique. - A long terme on observe des tableaux d'asthénie générale ou musculaire, céphalées, nausées, baisses de performance, voire troubles de la personnalité, confusion... Les horaires d'apparition de ces symptômes peuvent mettre sur la voie (coïncidence avec les heures de travail, rémission pendant le week-end ou inversement selon que la source est professionnelle ou domestique), ils peuvent aussi induire en erreur, évoquant des troubles plutôt psychogènes, d'autant plus qu'ils peuvent s'accompagner d'un syndrome dépressif. - A long terme, les faibles taux de HbCO sont suspectés d'être à l'origine du risque athéromateux observé chez les fumeurs. - L'incidence ou la prévalence de l'intoxication chronique au CO est parfaitement inconnue. Devant des céphalées, une asthénie, des vertiges ou nausées, troubles qui en l'absence de signes objectifs peuvent couramment passer pour psychosomatiques, voire dépressifs ou gériatriques, il faudrait avoir le réflexe d'un interrogatoire orienté. Pour exemple nous pouvons noter que pour les 10 années (1984 à 1993), 33 cas seulement d'oxycarbonisme chronique professionnel ont été pris en charge sur toute la France. - Au niveau cardiovasculaire -Bien que le CO soit considéré comme dénué d’effet toxique cumulatif sur le long terme, une action toxique à long terme sur le système cardio-vasculaire et neurologique ne peut être exclue. Il est possible que des facteurs génétiques et alimentaires modulent ce pouvoir pathogène ; des phénomènes compensatoires pourraient aussi intervenir. -Chez l’homme, les seuls effets chroniques qui ont été décrits sont consécutifs à des expositions aiguës lors d’intoxications accidentelles, ou des données collectées par la médecine du travail chez des sujets tabagiques. Il n’existe pas de données disponibles sur l’existence d’effets chroniques suite à une exposition de longue durée à des niveaux engendrant des taux d’HbCO inférieurs à la valeur de 2,5%, considérée par la plupart des auteurs comme ne devant pas être dépassée pour préserver les effets sanitaires. - D’après les données cliniques collectées par la médecine du travail et chez des sujets à forte consommation de tabac, la présence de HbCO pourrait être également un des facteurs favorisant la maladie athéromateuse et l’infarctus du myocarde. Des expérimentations animales ont montré que la présence de HbCO à un taux de 15% environ favorise la fixation du cholestérol sur les artères contribuant ainsi au développement d’athérosclérose. - Au niveau neurologique Le CO stimule le débit sanguin cérébral et diminue la vitesse de conduction nerveuse pendant et après l’exposition. Les lésions observées sont de type œdème généralisé, vacuolisation et démyélinisation. Ces signes sont surtout fonction de l’hypotension et de l’acidose lactique. - Effets sanitaires génotoxiques et cancérogènes Les données disponibles sur cet effet sont peu nombreuses et ne permettent pas de conclure sur le potentiel génotoxique du CO. Aucune donnée ne permet en l’état actuel des connaissances de suspecter que le CO puisse être une substance cancérogène. PRINCIPAUX GROUPES À RISQUE- les personnes présentant des pathologies cardiovasculaires :
- Le fœtus :
- Les enfants :
- les femmes enceintes :
- Les personnes présentant des pathologies pulmonaires obstructives (bronchite chronique ou emphysème) :
- Les personnes souffrant d’anémies ou d’hémoglobinopathies :
- Les personnes sous certains traitements médicamenteux :
- Interaction Chez l'humain
Relation dose-réponse
De nombreux modèles mathématiques ont été élaborés. Le modèle de Coburn-Foster-Kane (CFK), plus communément appelé modèle de Coburn ou modèle CFK (1965), est le plus pertinent d’entre eux. Il représente la meilleure façon de décrire la relation qui existe entre la concentration ambiante de monoxyde de carbone et le niveau de carboxyhémoglobine, chez des sujets soumis à diverses conditions. Les facteurs physiologiques et physiques appropriés y sont considérés. Mentionnons entre autres :- la concentration de monoxyde de carbone inhalé, la ventilation alvéolaire minute au repos et à l'effort physique;
- la production endogène de monoxyde de carbone;
- le volume sanguin;
- la pression barométrique;
- la capacité relative de diffusion des poumons.
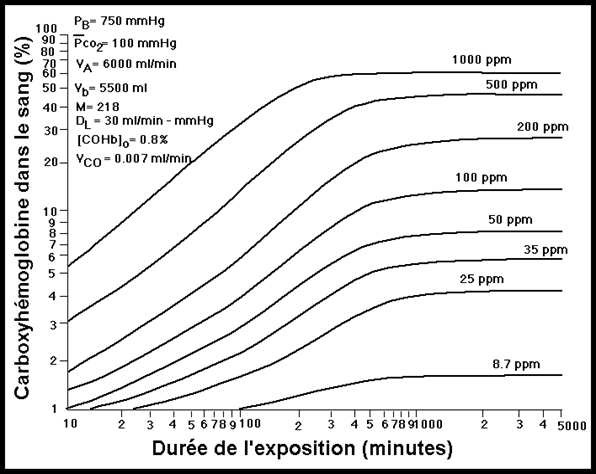
- La concentration de CO.
- La durée d’exposition
- La ventilation du sujet (fréquence et volume de la respiration).
- La sensibilité du sujet (Les personnes ayant des problèmes cardio-vasculaires sont très sensibles au CO).
- 5 heures en air ambiant.
- 90 minutes en atmosphère d’oxygène pur normobar.
- 20 minutes en atmosphère d’oxygène hyperbare à 3 ATA (OHB).
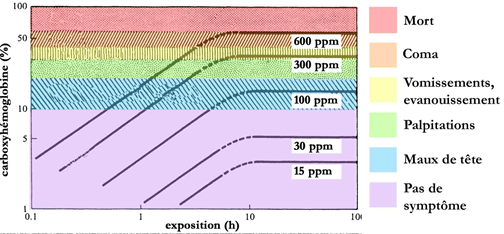

TRAITEMENT
- Eviction immédiate de l'atmosphère toxique (extraire la victime de l’atmosphère confinée l’amener immédiatement à l’air frais, aérer la pièce, fermer le compteur ou ne rien toucher d’électrique) -Ventilation à l‘O2 100% par masque, sonde naso-pharyngienne ou tube endotrachéal à fort débit (15 l/minute) (au plus tôt sans attendre les résultats) pendant 6h (l'O2 à 100% réduit le temps de demi-vie du HbCO de 3–5 h à 0,5–1 h). - Prélèvement sanguin pour dosage de CO et de HbCO (sang veineux ou artériel) en notant si le patient à reçu de l’O2 au préalable -En cas d’intoxication grave, transport rapide vers un centre disposant d’une chambre de traitement à l‘O2 hyperbare (OHB; ~3 atm). Ce procédé augmente le taux d'oxygène dans le plasma sanguin et accélère la séparation du CO et de l'hémoglobine. -L'élimination du monoxyde de carbone dans le corps humain dépend du taux d'oxygène dans l'air et de la pression atmosphérique.
- concentrations de HbCO >40%,
- tous les patients sans conscience et/ou présentant d’autres symptômes neurologiques (convulsions),
- Femme enceinte quelque soit le taux de CO et la symptomatologie
- enfant
- signes cardiaques ischémiques persistants.
TOXICOLOGIE ANALYTIQUE
L’analyse du monoxyde de carbone a deux visées distinctes mais complémentaires pour le diagnostic d’une éventuelle intoxication : l’une biologique te l’autre environnementale.- INDICATEURS BIOLOGIQUES
- formation endogène : 0,1 à 1,2 %;
- femme enceinte : 0,4 à 2,6 %;
- patients souffrant d'anémie hémolytique : 4 à 6 %;
- population urbaine : 1 à 2 %;
- voyageurs sur des autoroutes congestionnées : 5 % et plus;
- fumeurs :
- 1 paquet par jour 5 à 6 %,
- 2 à 3 paquets par jour 7 à 9 %,
- cigare jusqu'à 20 %;
- exposition à 50 ppm de chlorure de méthylène pendant 8 heures : 1,5 à 2,5 %.
- Pour une exposition de l'ordre de la VME (50 ppm), la concentration d'HbCO est de 3 à 4 % en fin de poste de travail.
- inférieure à 0,4 ml pour 100 ml de sang (0,18 mmol/L) chez les non-fumeurs ;
- entre 1 et 2 ml pour 100 ml de sang chez les consommateurs de 20 cigarettes par jour.
- population générale CO dans l'air de fin d'expiration : moins de 2 ppm chez les non fumeurs
- 30 à 50 ppm chez les fumeurs de 1 à 3 paquets par jour.
- INDICATEURS ENVIRONNEMENTAUX
- Dilution sanguine au 1/5.
- Tampon PH=5.35 (PH optimal : Toute l’oxyhémoglobine est précipitée et tout la carboxyhémoglobine est en solution).
- Chauffage au bain marie =55°C pendant 5’.
- Filtration : récupération de la carboxyhémoglobine qui est coloré .
- Lecture par rapport à une courbe d’étalonnage : coloration proportionnelle à la concentration de carboxyhémoglobine.

| Indicateur | Méthodes | Avantages | Désavantages |
| Discordance entre la PO2 du gaz artériel et la saturométrie | Utilisation occasionnelle en clinique | Peu spécifique Très peu sensible | |
| Réaction chimique | Simple | Résultats variables Technique désuète Peu rapide | |
| Carboxyhémoglobine | Spectrophotométrie (co-oximètre) | Peu dispendieux Relativement facile à faire selon les techniques Rapide Peut être automatisé | Résultats moins fiables pour carboxyhémoglobine < 2.5 % |
| Chromatographie en phase gazeuse | Sensible et reproductible Test à utiliser pour carboxyhémoglobine < 2.5 % Test étalon | Test laborieux Dispendieux Nécessite beaucoup de sang |
| Indicateur | Méthodes | Avantages | Désavantages |
| Air alvéolaire | Mesure CO par cellule électrochimique ou spectromètre infrarouge | Non invasif Rapide et facile Mesures peuvent se faire sur le terrain Bonne corrélation (.98) | Nécessite la coopération du patient Résultats peuvent être affectés par l’alcool et une déficience en lactase |
| Tubes colorimétriques | Non invasif Rapide et facile Résultats immédiats | Manque de précision Interférences avec d’autres gaz |

- Tubes réactifs
- Capteurs électroniques.
- Badges sensibles.
![]()
NORMES ET VALEURS SEUILS
Recommandations en milieu de travail| Organisme Concentration de | CO (ppm) | Durée |
| Occupational Safety and Health Administration (OSHA) | 50 TWAa | 8 heures7 |
| National Institute for Occupational Safety and Health (NIOSH) | 35 TWA 200 TLVb | 8 heures valeur plafond |
| American Conference of Governmental Industrial Hygienists (ACGIH) | 25 TWA | 8 heures19 |
| Règlement sur la qualité du milieu de travail (Québec) (RQMT) | 35 VEMPc 200 VECDd | 8 heures 15 minutes, pas plus de 4 fois/j2 |
| Organisme Concentration de | CO (ppm) | Durée |
| Santé et Bien-être social Canada (1989) | 25 11 | 1 heure 8 heures |
| Organisation mondiale de la Santé (OMS) (1987) | 90 50 25 10 | 15 minutes 30 minutes 1 heure 8 heures |
| American Society of Heating, Refrigerating and Air-conditioning Engineers (ASHRAE) | 9 | 24 heures |
| Environmental Protection Agency (EPA) | 35 9 | 1 heure 8 heures |
Was this article helpful?
YesNo
Last modified: 3 avril, 2018


